2030年中国帕金森疾病患者将超美国?为什么?
在研究人脑讯息传递方式长达 25 年后,2013年因为发现了人体细胞内的运输机制之谜、更准确说是细胞信息组织传递的机制,斯坦福大学分子与细胞生理学教授托马斯•苏德霍夫(Thomas C。 Südhof)获得了 2013 年诺贝尔生理学或医学奖。

其实,苏德霍夫教授最初想成为一名医生救人治病,但是他在学习的过程中逐渐感觉到,医生知道如何替病人解除痛苦,但是对疾病产生的深层次原因却知之甚少,那,为什么不先从根源了解起,看看人为什么会生病呢?
今天,硅谷洞察联合营创学院,为大家带来诺贝尔奖得主、美国科学院和美国医学科学院双院院士苏德霍夫教授一堂精彩课程:《生物制药的前沿科技探索》。
通过这堂课,让你迅速了解到底研究人的大脑对治病、生物制药有何帮助?当前人类大脑研究的挑战在何?又有什么工具和新进展?

(苏德霍夫教授在给营创学院EMBA学员上课中,版权属于营创学院)
从医生到科学家转变的背后
用苏德霍夫教授自己的话说,最早自己想要成为一名医生治病救人。因此 1982 年他就在德国哥廷根大学获得了医学博士学位(MD),同时,也获得了神经化学博士学位。
但是,既然治病需要研究发病机制,为什么不从根本上开始研究呢?“这也是我为什么对科学产生了兴趣的一个主要过程。”苏德霍夫教授表示。这里说的医学更偏重临床医学这一工程学科,而苏德霍夫教授指的从根本上研究发病机制,更偏向于生理学的科学范畴。
1983 年,苏德霍夫前往美国德州大学西南医学中心进行博士后研究。当时师从的两位大家,就是后来在 1985 年诺贝尔生理学或医学奖得主 Michael Brown 与 Joseph Goldstein 教授。

(左为Michael Brown教授,右为Joseph Goldstein教授,
这两位教授获得诺贝尔奖的理由就是因为发现了调控人体血液和细胞内胆固醇代谢的LDL受体以及胆固醇的代谢机制。
简单来说,就是他们发现低密度脂蛋白胆固醇 LDL 是一种 “坏” 胆固醇,当人体血液中这类“坏” 胆固醇升高,就会显著增加人心脏动脉硬化风险,从而导致各类心脏疾病并发症和死亡。在欧美发达国家,动脉粥样硬化更是导致疾病和死亡的主要原因。仅美国在 2005 年就有约1600 万冠状动脉粥样硬化性心脏病患者。
而这两位教授获诺奖的研究,正是 “科学推动工程学科发展” 的绝好例子:基于两位的发现,一种降脂类药从上世纪 90 年代开始研制,并在临床上得以广泛应用。这款药就是进入人体血液调节胆固醇浓度,从而降低动脉硬化风险。
苏德霍夫教授回顾这段历史时指出,这也是科学跟工程学科的一大不同。科学是为了回答问题,比如:为什么胆固醇会导致动脉硬化,胆固醇在血液内如何代谢,才能降低心脏疾病风险。解答了本质问题后,工程学科就要动手解决问题了,造出能解决疾病的药物,并通过各类临床检测到最终上市,从而造福病人。
同理,了解人体大脑内细胞的信息运转机制,也是从根本上了解到底大脑为什么发病,从而让生物制药界制造出能“对症下药”的药物。这也是苏德霍夫教授过去 25 年来致力研究的领域。
人的大脑:最难了解的器官
那么,到底苏德霍夫教授研究的具体内容是什么呢?
前面说过,苏德霍夫教授获诺贝尔奖的理由是发现了细胞信息组织传递的机制。也就是说,人体是如何通过讯号传递物质,从一个神经细胞传递到另一个神经细胞。苏德霍夫教授在其中揭示了一大要素:即钙离子是如何调控这整个过程的。
人体每个细胞如同一座工厂,制造和输出着各类分子比如胰岛素,产生后释放到血液中,而被称为神经传递素的化学信号则通过一个神经细胞传递到另外一个神经细胞。这些分子都被运输到细胞周围的被称为囊泡的小“包裹”中。
但是,什么时候,囊泡才会释放这些内容呢?只有当神经细胞向邻居发出信号时,才被允许释放它们的内容物。这过程中就受到钙离子的调控,触发囊泡的融合。因此,苏德霍夫教授的研究解释了细胞是如何准确地控制讯号传递物质的释放时机的。
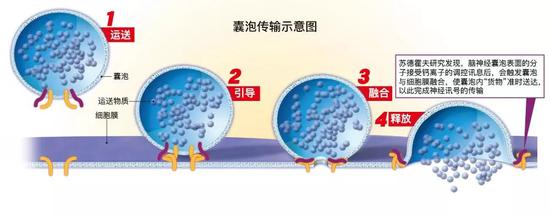
(硅谷洞察制图)
为什么说这项发现影响重大?
按照诺贝尔奖委员会的说法,三位获奖者揭开了细胞物质运输和投递的精确控制系统面纱,因为该系统的失调会为人体带来有害影响,可导致诸如神经学疾病、糖尿病和免疫学疾病等的发生。这无形中促进了对其它疾病的认识和研究。

(截图自诺贝尔奖委员会页面,最右为苏德霍夫教授)
这些神经细胞的传递,跟人体大脑又有啥关系?
神经细胞,又称神经元,是构成人体神经系统结构和功能的基本单位,神经细胞之间靠突触进行沟通,这也正是人脑能够运行的基础。苏德霍夫教授的研究就是搞清楚神经元之间的“通讯”是如何进行的。
苏德霍夫教授坦言,大脑可以说是人体最难了解的器官。对比一下人类的基因组数量就知道了。人的DNA数量是10的9次方,即10亿级别的。但大脑神经元数量是10的12、15甚至16次方,可以达到千亿个神经元。所以说,大脑远远超过了基因组的复杂程度,这也意味着基因组不可能完全决定大脑结构。
大脑是如何处理信息的的呢?神经元网络通过神经突触,形成一个神经回路。大脑不仅仅在其中传输信息,而且处理信息,就好比一个计算机的微型处理器一样。所以说,理解大脑如何处理信息,对理解人类的交流至关重要。
那么,脑部疾病研究当前的挑战在何?
在上个世纪,医学界最关心的疾病是什么? 毫无疑问,是癌症和心血管疾病。但是,苏德霍夫教授指出,这些疾病终究会得到控制,但是随着人类的生活质量越来越高,老年群体急剧增加,这会给医学行业带来一个新的、且需要极度关注的疾病,那就是——脑部疾病。
的确,大多数老年人疾病,都跟脑部疾病相关:
比如神经精神疾病(Neuropsychiatric)像抑郁症、自闭症、精神分裂症;还有神经退化性疾病(Neurodegenerative):比如阿尔兹海默症、帕金森症;癌症,比如胶质母细胞瘤(glioblastomas);神经血管疾病(Neurovascular)像中风、癫痫以及多发性硬化症等多种疾病。苏德霍夫教授指出,有统计预计,中国更是在 2030 年将会超过美国,成为帕金森患者最多的国家。
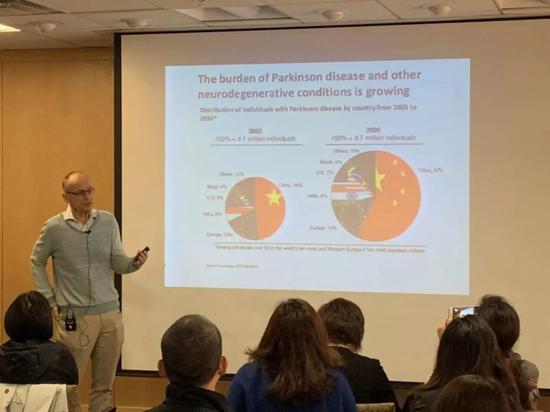
(2030年中国会超越美国,成为帕金森疾病患者最多的国家)
但现实中,大脑的疾病却并没有得到很好的重视,也很难治。为什么大脑疾病很难治呢? 主要原因在以下几点:
第一,大脑细胞不会增加。无论是刚出生的孩子还是100岁的老人,脑细胞的容量是一样的。一个人天生就具有的神经元数量,也将是一个人这辈子拥有的神经元数量,并不会随着年龄有所改变。
第二,脑细胞有着很长的传递距离,神经信号传递之间沿着的一条线路——即轴突(Axons),有多长呢?苏德霍夫教授比喻,这距离约32公里。如果说绕故宫跑一圈大约6公里的话,得跑上5圈。很长的同时,轴突也很细。这意味着,如果缺乏蛋白质合成的话,细胞之间的连接点—突触前终末(presynaptic terminal)会死掉。事实上,在有脑部疾病的患者当中,突触就会首先退化。
第三,脑细胞脆弱,容易退化,而且一旦脑细胞死掉则无法复制,脑部运动的复杂机理也导致了一个地方出错,整个神经网络可能就出错了。因此,大脑才是一个非常复杂的有机体。
面对众多脑部疾病,苏德霍夫教授认为,当前要”对症下药”的最大挑战有两点:第一点,如何把一款药制造出来, 即发现了解决病症的科学原理后,必须是可被制成药的(druggable);第二,成为药物后,要精密地控制药物的影响范围,不至于病人吃一颗关于脑神经的药物,却影响了整个下肢体的感觉。两者都十分重要。
当然,苏德霍夫教授笑称,为什么如今医学界会花费100倍费用在癌症研究,而不是在大脑研究呢?因为人类害怕癌症胜过于脑部神经错乱疾病的发生:“当你得癌症的时候,你知道你自己得了癌症。但当你疯的时候,你或许已经不知道了。”
生物制药开发的工具和进展
那么如何找到脑部疾病可制药的靶点(target)?苏德霍夫教授认为,现有医学界确实有不少新技术的出现,有助于药物开发。主要包括:干细胞生物学;基因编辑技术;转录组学;结构生物学(把药物放大至原子结构进行研究)等。
据苏德霍夫教授介绍,像干细胞技术,尽管当前并没有成为治疗疾病的技术,但对于科学家来说了解疾病的发病原理是很有用的。基因编辑技术可以很快检测基因中的疾病、变异,在人体如何表达。这些工具都是研制新药的基础。
但是,苏德霍夫教授也指出,能够用作药物开发的工具,并不意味着能用在人身上,比如前一阵子非常激烈讨论的基因编辑技术,就需要慎重对待。
对于制药领域而言,另一个不得不提的进展是:药物的种类发生了很大变化。从上个世纪50年代至今,药品的种类大致经历了以下几个阶段的发展:
从第一种药物研发至今,已经超过100年了。1950至1990年代,是属于小分子药(Small Molecules)的年代,90年代达到巅峰。像我们如今常见的阿司匹林、布洛芬等药物,就是小分子药。而且,现今大部分药品还是小分子药。
小分子药优点较多:很容易生产,也容易大规模复制,所以价格上也比较便宜,适用人群较为广泛。但缺点是,副作用很大,不够精准。
从上世纪70年代开始,蛋白质、多肽类药物等生物制剂(Biologics)出现。因为容易预测副作用,可以控制影响的范围,所以,如今大部分抗癌药都是生物大分子制药。因为生产成本高,销售价格高,自然利润空间就大,因此大型制药公司也比较喜欢生物制剂药物。
据统计,在 2010 至 2017 年期间,美国食品和药物管理局(FDA)批准了总共 262 个新分子实体药物(New Molecular Entities,NME),它们中有76%是小分子药物(199),只有四分之一是生物制剂。
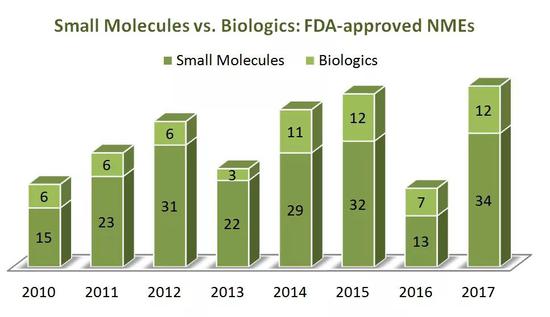
(Small Molecules:小分子药;Biologics:生物制剂,FDA批准的新分子实体药物数量)
如果从总体销售额和收入增长来看,情况则有所不同:2011年至2017年期间,生物制剂销售收入增长了70%,达到2320亿美元。生物制剂占整个医药市场的份额从 2006 年的 16% 上升到 2016 年的 25%,并没有明显放缓的迹象。
苏德霍夫教授指出,这当中无法回避的就是,生物制剂类药物前期生产成本偏高,难以标准化,同时无法进入大脑,对大脑无效。
从 2010 年起,新的趋势出现了:即 DNA/ RNA 以及细胞治疗技术。事实上,从上面分子级别,到蛋白质级别的药,再到细胞、基因级别的药物,正是在不断深入疾病的核心,控制疾病的进程。从治疗症状到治疗疾病的核心。不过目前,相关的基因疗法尚未被 FDA 批准,主要是因为耗资太大,开发过程很繁复,所以如何筹集足够多的资金来研发,是一大难题。
苏德霍夫教授认为,这类基因类的、细胞治疗药物,主要通过基因、核酸去延缓疾病的发展,在未来数十年会越来越重要,可以说是制药的未来。现在制药公司主要关注在癌症,以及罕见病的药物开发,脑部疾病相较于两者,重视程度仍有待提高,也期待全社会的共同关注。
标签:
相关阅读
404 Not Found
精彩推荐
404 Not Found
阅读排行
404 Not Found
相关词
- 世界新资讯:君禾股份:未来预期随着海外库存消耗及消费市场逐步复苏 水泵主业会呈现复苏反弹
- 2023山西太原市古交市招聘社区专职社工体检和考察公告_天天时快讯
- 易纲:坚决把绿色金融工作摆在突出位置,实现“3060”目标需要胡萝卜加大棒
- 2023年山东泰安肥城市城市社区专职工作者招录进入面试范围人员递补名单(第三批)_时讯
- 每日看点!隔夜SHIBOR报1.3390% 下降6.50个基点 7天SHIBOR报1.8500%
- 世界快播:华菱钢铁:目前废钢资源相对稀缺成本较高,长流程炼钢更具经济性
- 全球消息!易会满:进一步打通痛点堵点,为机构投资者入市创造更加有利环境
- 《神秘岛》开发商新作《苍穹乾坤》使用AI辅助开发 引众筹者不满
- 天天头条:五大行再次下调存款利率
- 客人去哪了?五一后各地餐饮生意直线下滑,突然就没人了
- 当前快看:理想汽车在青岛成立销售公司
- 潘功胜:中国稳健金融周期为经济和金融市场运行提供适宜环境
- 美国社交电商再起波澜:TikTok商城开张,Meta却要闭门做生|今日快看
- 世界快资讯:上海再保险“国际板”正式启动
- 特别好评RPG游戏《恐怖的世界》 完整版10月19日上线|环球精选
- 易会满:持续加大对伪私募、地方交易场所等重点领域风险的整治
- 十元店重回巅峰:新穷人与日本1990s
- 每日快报!教育股震荡走低 国新文化跌超8% 荣信文化跌逾7%
- 全球快讯:央行潘功胜:人民币债券具有良好的投资组合分散化价值
- 国产大飞机开启常态化商业运行:C919带动产业链一起飞 市场规模有望达万亿元量级
- U盘安装系统时蓝屏怎么解决 全球头条
- ROG蓝屏后该采取什么解决方法来重启 世界快报
- 中国地震局:国家地震烈度速报与预警工程已完成主体建设任务 焦点讯息
- win10启动就蓝屏是怎么回事 全球热点
- 环球头条:华硕笔记本acpi蓝屏该如何解决
- 世界最资讯丨打击违规销售作弊器材行为 海南省市场监管部门多措并举为高考中考保驾护航
- 每日热议!永劫无间蓝屏死机应该如何处理
- KMODE蓝屏出现应该如何处理 全球观热点
- 携程集团发布2023年第一季度财报
- 甘肃省华亭市东华镇市场监管所开展农村夏季食品安全专项检查_环球热资讯
- 深圳市市场监管局总部经济审批服务“全市通办”正式落地
- 解码开化(一) 文旅产业:从“高看一眼”“棋高一招”到“焕然一新”
- 第五届京津冀石墨烯大会在北京房山举办,加速三地产业链深度融合
- 高考期间海南天气如何?未来两天多云有雷阵雨 焦点速读
- 别被“蚊蝇通杀”迷了眼
- 啥是海洋?直播带你一起看 天天快看点
- 内罗毕:低碳和电动交通载具展 天天观速讯
- 环球播报:斯诺克新星赵心童为涉赌遭禁赛道歉
- 《沙石镇时光》:1.0版本发售日期公布!通过“塑造你的未来”预告片为前方的秘密和危险做好准备 世界独家
- 关注眼健康亟须全社会行动起来
- 哈利波特魔法觉醒怎么尊享眉色 尊享眉色方法攻略 环球速看
- 甘肃省华亭市市场监管局多举措保障中高考期间食品安全 环球新动态
- 第19届深圳文博会人气旺 每日快报
- 甘肃省嘉峪关市市场监管局镜铁分局全力保障高考期间食品和特种设备安全
- 河北沙河:太行古村落焕发新活力_天天快播
- 世界百事通!晋陕峡谷遇奇石
- “共建首都跨境电商新生态”系列活动在京启动 每日热门
- 环球看热讯:汉字工坊上班不带饭怎么过 找出9个公司吃的答案分享
- 甘肃省张掖市新墩市场监管所“三力齐发”加强中高考期间特种设备安全保障_环球热推荐
- 快消息!小心,这种眼疾易盯上上班族
- 眼药水怎样使用才正确
- 当前讯息:机器人:公司基本实现了35kg以下新款机器人减速器的国产化替代
- 华菱钢铁:钢材产品在新能源新材料领域需求前景将持续向好-天天通讯
- 今早发布!雷雨!_天天即时
- 全球快报:云顶之弈s9暗影岛格温阵容攻略 s9赛季暗影岛格温阵容搭配
- 江苏“智造”夯牢实体经济“家底”
- 加拿大野火烟尘飘至美国 部分地区被烟尘笼罩
- 【环球时快讯】文字玩出花无法原谅怎么过 无法原谅十二处细思极恐在哪
- 环球快播:百亿授信!民生银行与协鑫集团达成全面战略合作
- 前5月外贸保持稳定增长 制造业转型升级塑造出口新动能
- 简讯:江苏油田页岩油累产突破4万吨
- 让城市成为“开放的艺术馆”(金台随笔) 视点
- 易会满:适时出台资本市场进一步支持高水平自立自强的政策措施 全球报道
- 【全球聚看点】河南麦收进度过八成 夏播已完成近五成
- 今起,在锡启幕!
- 两大国际组织上调中国2023年经济增长预期
- 仲景食品:公司产品以国内销售为主 出口业务占比较小-每日速看
- 天天速递!U盘装系统进入PE蓝屏该采取什么解决方法
- 充满算计!日美澳在南太铺光缆,日媒炒“抗衡中国影响力” 焦点热门
- 重点聚焦!力箭一号火箭的专属发射工位长什么样?
- 袁明辉:拍摄下来记录下来用自然摄影留住那些美好
- 扫码支付已在国内迅速发展普及 刷掌支付是否还有市场前景
- “去风险”成脱钩新马甲
- 环球微资讯!360qpesv.sys导致蓝屏该采取什么解决方法
- 【新要闻】北海市海城区地角街道辖区率先完成第二季度食品安全“两个责任”包保工作
- 国家开发银行前5个月发放交通领域贷款2687亿元
- 当前视点!带火原料药企,马斯克加持的“减肥神药”又火了
- 什么是股份制企业?股份制企业和私营企业的区别有哪些?
- 怎么才能正确安装python39.dll
- 全球连线|对两国合作机遇充满期待——洪都拉斯各界热议中国驻洪使馆开馆
- 兰州新区召开第二季度落实食品安全“两个责任”推进会议
- 民泰银行绍兴分行创新产品助共富系列① | 动产融资业务,为民播下“共富”希望-世界实时
- 【世界快播报】我国外贸连续4个月保持正增长
- 偷渡罪一般判多少年?偷渡人员怎么正规回国?
- 吉利雷达以“真乘用化”撬动市场,5月销售1016台创历史新高 焦点资讯
- 故意伤害致人死亡如何处罚?故意伤害致死赔偿多少?
- “6·6”全国爱眼日公益讲座在京举办
- 上古诸神:卡牌对战官网在哪下载 最新官方下载安装地址 环球热推荐
- 天天头条:电脑中缺失alrsvc.dll文件应该怎么处理
- 赡养费标准是什么?不给赡养费最严重的后果有哪些?
- 只允许跟院方合作民营救护车辆进入?医院回应
- 涉案金额959万元!海口曝光9家定点医疗机构
- 世界快播:如何解决电脑端丢失rasmans.dll提示问题
- 微资讯!江西省新余市市场监管局:强化建材质量监管 守牢质量安全防线
- 【快播报】警惕“负首付”骗贷
- 财产税有哪些税种?所得税和财产税的区别有哪些?
- 高考第二天部分地区已公布查分时间 胜利在望,加油少年!|全球快看点
- 青海省海西州四项措施为“中高考”保驾护航_每日看点
- 嫖娼拘留多少天?初次涉黄拘留几天?
- 青海省市场监管局发布中高考期间食品安全消费提示 天天热门
- 浙江金华婺城区:天然富硒,“硒”望之旅
- mtfutils.dll缺失如何恢复
- 忘了车限号开了一天罚多少钱?郑州限行免罚有几次机会?
- 焦点快播:网红化妆大师官网在哪下载 最新官方下载安装地址
- 动态:量子密钥分发攻防研究获重要进展
- 什么是违法所得?违法所得和非法财物的区别有哪些?
- 仙迹之九州神剑官网在哪下载 最新官方下载安装地址|今热点
- 工程预付款是怎么规定的?工程预付款为什么要扣回?
- 种一颗牙便宜多少钱?海南打出种植牙降价“组合拳”
- 劳动合同法第38条是什么内容?公司不辞退故意调岗怎么赔偿?
- 无证驾驶怎么处罚?无证驾驶会被马上拘留吗?
- 当前时讯:生存冒险游戏《血清》新预告 拥有4人合作模式
- 天天观热点:岭南街道构建“一网二联三队伍”服务模式,为社区长者健康保驾护航
- 通信业全力保障高考|莘莘学子逐梦未来 通信业全力护航
- 焦点观察:华为品质宽带智能运维系统荣获CAICT光接入网L3.5等级认证
- 青海省启动“企业商业秘密保护能力提升服务月”活动-天天速看
- 黑龙江省北安市市场监管局着力打造“帮您办”服务品牌|动态焦点
- 非遗 | 高校留学生走进安徽文旅扶点-环球通讯
- 今日快看!FPS游戏《无畏契约》国服今日终测 删档充值返利
- 环球最新:黑河联通多措并举提升廉洁文化教育质效
- 每日视点!语文名师点评AI高考作文:百度搜索AI伙伴优于New Bing、ChatGPT
- 国家金融监督管理总局李云泽:正式启动上海再保险“国际板”-环球快看点
- 全球报道:重庆油菜喜获丰收 总产量实现连续16年增长
- 冒险游戏《血清》发布实机视频 支持简体中文 四人联机
- 全力保障高考通信畅通,重庆电信在行动!_环球速读
- 《无人深空》发布季节性更新“奇点”预告视频 现已正式上线-环球微速讯
- 世界殿堂级名团重返中国舞台 玛莎·葛兰姆现代舞团尽展风采 观速讯
- 上海移动获得DC-Tech数据中心智能建造最高等级认证 当前快讯
- 戴尔电脑开机后蓝屏重启应该怎么应对
- 电视剧《照亮你》在都市类型中铺展新的叙事面向 世界要闻
- 黑白琴键抒写长三角风情 全球新要闻
- 上海世纪出版、米哈游、东方明珠新媒体上榜
- 电脑提示vcomp140.dll文件丢失的解决方法|环球新要闻
- 世界今热点:切实保护金融消费者合法权益
- 全球快报:电脑蓝屏nv1ddmkm.sys怎么办
- “拆楼”式装修必须叫停
- 世界今日讯!李云泽:下好风险前瞻防控先手棋,以更加主动态度应对风险隐患
- 湖北馆展品超5000件:五大“重器”显实力 五类“非遗”溢楚风_今日看点
- 国家金融监督管理总局李云泽:监管体制改革是金融改革的重要一环 天天快资讯
- 公安部交管局公布近期三轮车肇事肇祸典型交通事故案例
- 网传重组人生长激素进浙江集采 长春高新连夜召开电话会回应
- 当前通讯!传记文学《灵魂的旋律:我的父亲刘炽》:再现作曲家刘炽艺术人生
- 全球微头条丨欢乐家的椰子“野心”:去年椰子汁饮料营收超8亿,今年加码投资
- 腾势D9车型5月销量11005辆,环比增长约9.6%
- 两部门:举办全国和美乡村篮球大赛(村BA)
- 最新资讯:Win10 watchdog.sys蓝屏该采取什么解决方法
- 世界视讯!《神仙道3》神阙风物志第五章详细通关攻略
- 全球净零技术制造竞争全面展开 时讯
- 海口江东新区盛泰仕家安居房项目预计10月底全面封顶
- 刀具等特殊商品退货难邮寄,如何解?

















































